Kunci Jawaban IPA Halaman 116 Kelas 10 – Hai, kawan semuanya, salam giat belajar. Melalui konfigurasi elektron dari atom suatu unsur kita juga bisa mengetahui sifat kimia dan fisika yang spesifik pada unsur itu. Hal ini dinamakan sifat keperiodikan unsur.
Salah satu sifat keperiodikan unsur yang dibahas pada bab ini adalah jari-jari atom. Bagaimana cara menghitung jari-jari atom? terdapat simbol “r” yaitu jari-jari dan “d” merupakan diameter. Adapun jari-jari atom dinyatakan dalam satuan Angstrom (Å). Satu Å = 100 pm (pikometer). Satu pm besarnya sama dengan 10–12 m. Ukuran jari-jari atom berkisar 30 – 300 pm
Berikut jawaban tentang “Aktivitas 5.3”. Dengan adanya pembahasan ini diharapkan adik adik semuanya dapat memahami materi tentang Jari-jari Atom sebagai Sifat Keperiodikan Unsur.
Lebih baik adik adik membaca dan memahami materinya terlebih dahulu sebelum mengerjakan soal. Karena soal yang ada pada buku siswa berasal dari materi materi tersebut. Semakin adik adik sering membaca dan memahami materinya akan memudahkan dalam menyelesaikan soal- soalnya.
Setelah adik adik memahami materi barulah adik-adik mengerjakan soal yang terdapat dibawah ini. Sebelum adik adik mencocokkan dengan kunci jawaban yang telah kami sediakan, ada baiknya adik-adik mengerjakan dahulu soal tesebut secara mandiri maupun diskusi dengan teman.
Kunci Jawaban IPA Halaman 116 Kelas 10
Aktivitas 5.3
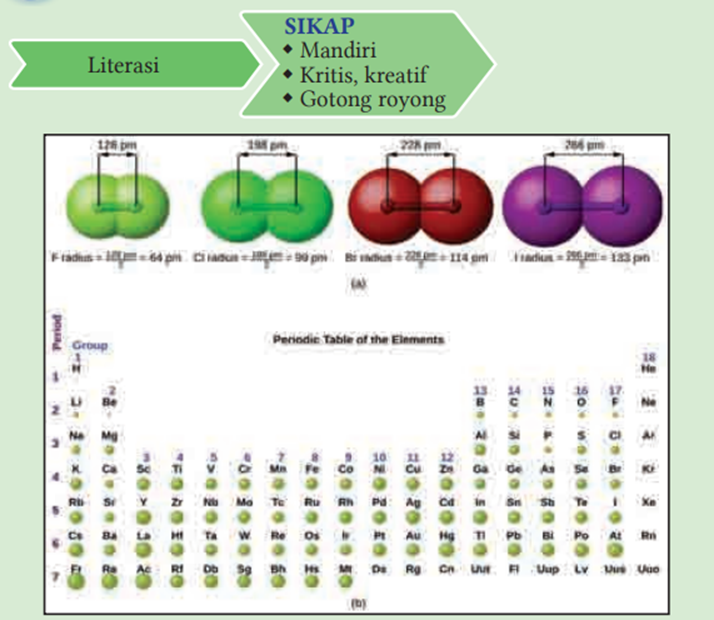
Bekerjalah dalam kelompok. Analisislah diagram pada Gambar 5.4. untuk menjawab pertanyaan berikut dan komunikasikan hasilnya dalam diskusi kelas.
1. Jelaskan bagaimana kecenderungan jari-jari atom dalam satu periode (baca: dari kiri ke kanan) jika dihubungkan dengan bertambahnya nomor atom?
Jawaban :
Kecenderungan jari-jari atom dalam satu periode dari kiri ke kanan adalah makin mengecil sebab meskipun jumlah kulit sama namun bertambahnya nomor atom adalah bertambahnya massa atom (proton) yang bermuatan positif. Dengan demikian terjadi gaya tarik-menarik yang lebih kuat antara inti atom yang bermuatan positif terhadap elektron valensi yang bermuatan negatif sehingga jari-jari atom memendek. Unsur dengan jari-jari atom terpendek adalah unsur He.
2. Jelaskan bagaimana kecenderungan jari-jari atom dalam satu golongan (baca: dari atas ke bawah) jika dihubungkan dengan bertambahnya nomor atom. Jelaskan unsur manakah yang memiliki jari-jari atom terpendek dan manakah yang terpanjang jari-jari atomnya
Jawaban :
Kecenderungan jari-jari atom dalam satu golongan dari atas ke bawah adalah makin membesar sebab bertambahnya jumlah kulit atom menambah panjang jarak dari inti atom ke elektron valensi. Gaya tarik-menarik antara inti atom dan elektron valensi pun melemah dengan semakin bertambahnya kulit atom. Hal ini akan membuat elektron valensi mudah lepas. Unsur dengan jari-jari atom terpanjang adalah unsur Fr
Penutup
Teman-teman, itulah pembahasan yang bisa berikut.id bagikan. Semoga bisa membantu teman-teman dalam memahami materi tersebut, Jangan lupa bagikan kepada teman-teman lain agar semakin bermanfaat!
Tetap semangat dan jangan lupa simak pembahasan lain di berikut.id ya!
Disclaimer:
1. Konten ini dibuat untuk membantu orang tua dalam membimbing anak dalam belajar, selayaknya dijelaskan proses penemuan jawaban, bukan hanya hasil akhir.
2. Jawaban bersifat terbuka, dimungkinkan bagi siswa dan orang tua mengeksplorasi jawaban lebih baik.
3. Artikel ini tidak mutlak menjamin kebenaran jawaban.
Baca Juga
Kunci Jawaban IPA Halaman 123 Kelas 10
Kunci Jawaban IPA Halaman 108 dan 110 Kelas 10
